Biorrobô: Água-viva artificial movimenta-se com células cardíacas
Redação do Site Inovação Tecnológica - 23/07/2012
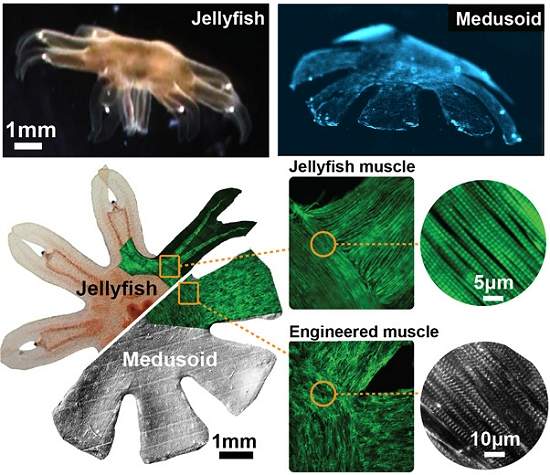
[Imagem: Nawroth et al./Nature Biotechnology]
Biomecânica
Cientistas juntaram proteínas e células vivas do coração de animais a uma matriz de silicone para criar uma água-viva capaz de se movimentar.
O feito serve como uma prova de conceito da engenharia reversa de seres vivos ou, pelo menos, de músculos e formas de vida simples.
Janna Nawroth e seus colegas das universidades de Harvard e Caltech afirmam também que sua "água-viva meio viva" amplia a definição da chamada "vida artificial", ou vida sintética, um campo emergente de pesquisas, baseado sobretudo na biologia sintética.
Assim, a água-viva biomecânica é menos robótica do que sua similar apresentada há poucos meses.
Seus criadores a batizaram de Medusoide, em referência a medusa, outro nome pelo qual as águas-vivas são conhecidas.
Engenharia de tecidos
"Um dos maiores objetivos do nosso estudo era fazer avançar o campo da engenharia de tecidos," disse Nawroth, referindo-se às tentativas de reproduzir tecidos vivos em laboratório, algo que, segundo ela, tem sido feito mais como uma arte, juntando componentes que se acredita serem importantes, mas sem necessariamente entender os princípios de funcionamento do tecido como um todo.
Entender e imitar a água-viva pareceu um objetivo natural, já que a ciência acredita ser esse um dos mais antigos animais da Terra dotados de múltiplos órgãos.
Esses animais usam seus músculos para bombear água e se movimentar, de uma forma muito similar com o pulsar do músculo cardíaco.
Biorrobô
Para criar sua medusa artificial, os pesquisadores começaram com um molde de silicone, desenvolvendo um formato que lembra ligeiramente o corpo do animal, e aprimorando-o para que não vazasse muita água entre as "pétalas", o que faria o biorrobô perder impulso.
A seguir, eles aplicaram uma camada cuidadosamente projetada de proteínas, tentando reproduzir ao máximo a arquitetura muscular do animal.
Essa camada de proteínas serviu como guia para o crescimento e a organização da camada seguinte, formada por células do coração de ratos.
Segundo os pesquisadores, para obter o movimento ritmado, ou pulsante, foi necessário combinar quantitativamente a arquitetura subcelular, celular e supracelular da musculatura da água-viva com as células cardíacas.
Isso abre caminho para exploração da técnica para a construção de órgãos artificiais ou, pelo menos, para o desenvolvimento de "remendos" para tecidos do corpo humano danificados por acidentes ou doenças.
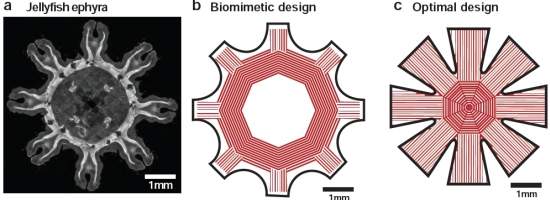
[Imagem: Nawroth et al./Nature Biotechnology]
Seres sintéticos
O "ser sintético" foi colocado em água salgada, à qual foi aplicada uma corrente elétrica alternada - entre 0 e 5 volts - que faz com que as células cardíacas pulsem, movimentando o biorrobô.
Na verdade, as células cardíacas já pulsavam ligeiramente sem a aplicação da corrente, mas geravam um movimento que não era forte o suficiente para movimentar o biorrobô.
"Como engenheiros, ficamos muito confortáveis em construir coisas de aço, cobre e concreto," disse o Dr. Kevin Parker, coautor do estudo. "Eu vejo as células como outro tipo de substrato de construção, mas precisamos de especificações quantitativas rigorosas para mover a engenharia de tecidos para um tipo reproduzível de engenharia."
Segundo Parker, enquanto a biologia sintética e sua busca pela vida artificial está "focada na manipulação genética de células, em vez de construir uma célula só, nós queremos construir uma besta".
Artigo: A tissue-engineered jellyfish with biomimetic propulsion
Autores: Janna C Nawroth, Hyungsuk Lee, Adam W Feinberg, Crystal M Ripplinger, Megan L McCain, Anna Grosberg, John O Dabiri, Kevin Kit Parker
Revista: Nature Biotechnology
Vol.: Published online
DOI: 10.1038/nbt.2269


Menor energia já medida permitirá contar fótons um por um
Nova técnica reprograma a matéria rearranjando rapidamente seus átomos
Gerador termoelétrico projetado por computador fica 8x mais eficiente
Computador alternativo de silício resolve problemas intratáveis hoje
Metapropulsão movida a luz pode nos levar às estrelas em 20 anos
Interação da luz com ondas gravitacionais pode detectar partículas de gravidade
Computação com luz pulsada atinge 10 THz
Metalurgia quântica manipula a matéria em escalas impensáveis
Células solares quase invisíveis para vidros de carros e janelas
Superinox: O aço que pode viabilizar Economia do Hidrogênio
Como criar robôs inteligentes como os da ficção científica?
Processador biológico-eletrônico usa células cerebrais vivas para computação
Chips cerebrais vão se dissolver depois de fazerem seu trabalho
Material tem rigidez alterada remotamente por ondas sonoras
Implante neural menor que um grão de sal consegue ler seu cérebro
Lavar frutas e verduras na banheira? É quase isso, só que melhor
Todos os direitos reservados.
É proibida a reprodução total ou parcial, por qualquer meio, sem prévia autorização por escrito.