Catalisador atômico quebra mais forte ligação do carbono
Redação do Site Inovação Tecnológica - 15/10/2018
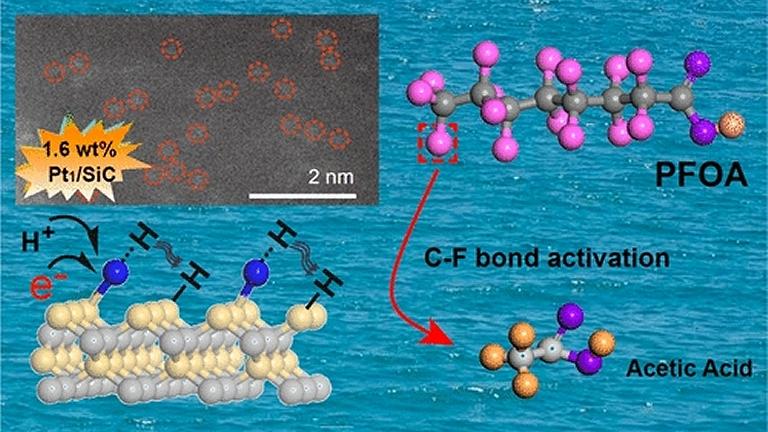
[Imagem: Dahong Huang et al. - 10.1021/acscatal.8b02660]
Catalisadores de átomo único
Uma equipe internacional de cientistas desenvolveu um catalisador atômico - o que, por si só, já é um avanço fundamental - capaz quebrar as ligações carbono-flúor, uma das mais fortes ligações químicas conhecidas.
A descoberta é um avanço para os esforços de remediação ambiental e síntese química.
"Nosso objetivo era desenvolver uma tecnologia que pudesse degradar as substâncias perfluoroalcóixidas (PFAs), um dos mais desafiadores problemas de remediação de poluentes dos dias atuais.
"As PFAs [resinas de polímero perfluoroalcóxico] são amplamente detectadas em todo o mundo, desde a biota ártica até o corpo humano, e as concentrações em águas subterrâneas contaminadas excedem significativamente o limite regulatório em muitas áreas. Atualmente, não há métodos energeticamente eficientes para destruir esses contaminantes. Nossa colaboração visa resolver este problema, aproveitando as propriedades únicas dos catalisadores de átomo único," disse o professor Jaehong Kim, da Universidade de Yale, nos EUA, acrescentando que essas resinas são mais conhecidas pelo seu nome comercial Teflon®.
Catalisadores menores e mais eficientes
Para otimizar a eficiência dos catalisadores - substâncias que iniciam ou aceleram as reações químicas - os cientistas dividem-nas em pedaços menores, indo até os nanomateriais. E recentemente, eles começaram a quebrar os catalisadores ainda mais, além da nanoescala e até em átomos individuais, incluindo átomos artificiais.

[Imagem: Dahong Huang et al. - 10.1021/acscatal.8b02660]
"A única parte de um catalisador que é reativa é a sua superfície," explica Eli Stavitski, do Laboratório Nacional Brookhaven. "Então, se você divide um catalisador em pequenos pedaços, você aumenta sua área superficial e expõe mais as propriedades reativas do catalisador. Mas também, quando você quebra os catalisadores abaixo de 10 nanômetros, suas propriedades eletrônicas mudam drasticamente. De repente, eles se tornam muito reativos. Em última análise, você quer ir para o próximo passo e dividir os catalisadores em átomos individuais. "
O desafio é que os átomos individuais não se comportam da mesma forma que os catalisadores maiores; eles não gostam de ficar sozinhos e podem causar reações colaterais indesejadas. Para utilizá-los na forma de átomos individuais é necessário encontrar a combinação perfeita entre um metal forte e reativo, como a platina ou o ródio, e um ambiente estável e complementar.
"Nossa equipe desenvolveu um método prontamente escalonável para sintetizar catalisadores de átomo único em duas etapas simples. Primeiro, ligamos os metais a locais de ancoragem em um material de suporte, então fotorreduzimos os metais em átomos individuais sob irradiação leve de UV-C.
"Usando este método, nosso grupo sintetizou um conjunto de catalisadores de átomo único envolvendo vários metais (platina, paládio e cobalto) e suportes (carbeto de silício, nitreto de carbono e dióxido de titânio) para inúmeras reações catalíticas. Neste trabalho, descobrimos que átomos de platina simples ancorados sobre carbeto de silício são notavelmente eficazes na catalisação da clivagem de ligações flúor-carbono e na quebra de contaminantes como as PFAs," disse Kim.
A equipe vai continuar a colaboração para aplicar os catalisadores de átomo único a vários desafios ambientais além das PFAs.
Artigo: Single-Atom Pt Catalyst for Effective C-F Bond Activation via Hydrodefluorination
Autores: Dahong Huang, Glen Andrew de Vera, Chiheng Chu, Qianhong Zhu, Eli Stavitski, Jing Mao, Huolin Xin, Jacob A. Spies, Charles A. Schmuttenmaer, Junfeng Niu, Gary L. Haller, Jae-Hong Kim
Revista: Catalysis
Vol.: 8, pp 9353-9358
DOI: 10.1021/acscatal.8b02660


Descoberto pequeno objeto com atmosfera nos confins do Sistema Solar
Visão de raios X enxerga dentro de chips em funcionamento
Como criar robôs inteligentes como os da ficção científica?
Gerador termoelétrico projetado por computador fica 8x mais eficiente
Metapropulsão movida a luz pode nos levar às estrelas em 20 anos
Potência dos lasers é multiplicada por espelho de plasma
O tempo é contínuo ou discreto? Relógios atômicos vão responder
Interação da luz com ondas gravitacionais pode detectar partículas de gravidade
Metalurgia quântica promete manipular a matéria em escalas impensáveis
Computação com luz pulsada atinge 10 THz
Hidrogênio e oxigênio são produzidos com um único átomo
Hidrogênio solar agora dispensa a caríssima platina
Vida pode ter emergido em géis da Terra primitiva
Emergência da vida na Terra é simulada em experimento
Planetas sem água podem ter vida baseada em líquidos iônicos
Chip filma e controla reação química em tempo real
Todos os direitos reservados.
É proibida a reprodução total ou parcial, por qualquer meio, sem prévia autorização por escrito.